北理工和UIC大学合作在大环内酯新作用机制发现方面取得重要进展
发布日期:2024-07-23 供稿:化学与化工学院 摄影:化学与化工学院
编辑:田柳 审核:王振华 阅读次数:
近日,必赢在线注册,(中国)科技公司化学与化工学院梁建华教授与美国伊利诺伊大学芝加哥分校核糖体生化专家Alexander S. Mankin教授和核糖体晶体结构学家Yury S. Polikanov副教授合作,在设计不同作用机制的抗耐药菌大环内酯取得重要进展。相关成果以“Macrolones target bacterial ribosomes and DNA gyrase and can evade resistance mechanisms”为题发表于国际顶刊《Nature Chemical Biology》。通讯单位是伊利诺伊大学芝加哥分校和必赢在线注册,(中国)科技公司,伊利诺伊大学芝加哥分校的Elena V. Aleksandrova, 必赢在线注册,(中国)科技公司化学与化工学院的博士生马聪璇和伊利诺伊大学芝加哥分校的Dorota Klepacki为共同第一作者,梁建华教授,Yury S. Polikanov副教授和Alexander S. Mankin教授为共同通讯作者。
目前临床半数抗生素作用于核糖体,核糖体的结构非常庞大和复杂,其结构和功能的解析在2000年左右取得突破,三位研究者万卡特拉曼-莱马克里斯南、托马斯-施泰茨和阿达-尤纳斯因此获得2009年诺贝尔化学奖。大环内酯类药物如红霉素、克拉霉素、阿奇霉素等因为其副作用少,安全性高被广泛用于上下呼吸道细菌性感染的治疗。然而抗生素的长期使用以及细菌的进化使得细菌耐药性日益严重,其中erm耐药基因表达的甲基化酶会导致骨架迥异的大环内酯类、林可酰胺类和链阳菌素B类的共同抗菌作用位点即核糖体A2058被甲基化修饰,这类交叉耐药性被称作MLSB类耐药。为了得到能够抗耐药菌且减缓细菌耐药突变的抗生素,使用药效团融合策略将大环内酯与喹诺酮连接得到的杂合物——“macrolone”有可能突破目前的MLSB类耐药,然而当前研究存在的局限性是:一方面目前其他课题组报道的大环内酯和喹诺酮的杂合物不具有双靶标模式,仍然只作用于核糖体;另一方面目前已知的抗耐药菌靶点为核糖体碱基A752-U2609,代表性上市药物是泰利霉素,但是其抗高水平耐药菌仍有很大不足,目前其他同质性抗生素未能获得上市批准,亟需针对耐药机制寻找新的核糖体作用位点。
近十余年来,梁建华团队在抗耐药菌大环内酯上不断迭代设计,从数百种抗耐药菌大环内酯中挑选了3种代表性的“macrolone”结构,与Yury S. Polikanov副教授和Alexander S. Mankin教授合作进行了机制研究。通过体内双基因报告(图a)和体外蛋白翻译转录抑制实验以及DNA超螺旋抑制实验确定三种结构的主要作用靶标是不同的,分别是MCX-91主要作用于核糖体、MCX-66主要作用于DNA促旋酶、MCX-128能够同时作用于核糖体以及DNA促旋酶。模式菌 Thermus thermophilus 核糖体与这三个化合物的高分辨率复合物晶体结构(分辨率是2.35Å-2.60Å)显示作用于核糖体的C2586-C1782新位点(图b),这与我们先前临床病原菌金黄色葡萄球菌(MRSA)核糖体与化合物MCX-190的复合物冷冻电镜结构解析结果一致(Cell Discovery, 2024, 10(75),DOI : 10.1038/s41421-024-00702-y)。两种不同的核糖体结构解析技术相互印证了我们的化合物在不同菌株中均能作用于新位点C2586-C1782;并且MCX-128对于A2058双甲基化的模式菌核糖体也能够紧密结合,证明了其较好的抗耐药菌的新模式。而后我们又对化合物的抑制蛋白质翻译特征以及是否诱导细菌产生耐药特性进行了研究,通过toeprinting技术对化合物抑制蛋白翻译的停止位点研究发现,传统红霉素允许翻译的肽链长度较长,而MCX系列化合物在翻译较短肽链时即可停止(图c);红霉素会诱导erm耐药基因表达,但MCX系列化合物则不会诱导耐药基因表达,因此MCX系列化合物具有不同于以往大环内酯的新作用模式。特别需要指出的是,化合物MCX-128具有双靶标作用机制,药物在使用过程中当单一靶标突变时,化合物MCX-128作用另一靶标则能够有效地抑制单靶标突变的菌株,使其无法幸存下来,因此在MCX-128对抗下细菌很难同时在核糖体以及DNA促旋酶同时发生自发突变(图d),而相比之下单作用机制的化合物MCX-66和MCX-91较容易产生突变菌株。这样既不容易诱导耐药基因表达,又不容易使细菌产生自发突变的药物在临床使用具有很大的优势。
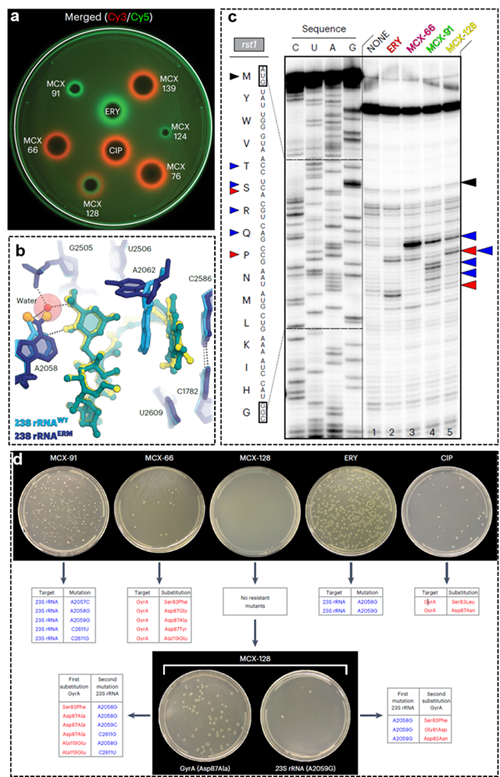
化合物的作用机制
该项研究证实通过合理药物设计能够控制大环内酯与喹诺酮杂合物的主要作用靶标,启发人们意识到药物设计的新化学空间。同时,我们基于核糖体的新作用位点创造性地设计了一个喹诺酮骨架药效团,使化合物既作用于核糖体新位点又作用于拓扑异构酶,一石二鸟。在本研究中,喹诺酮抗生素通过合理设计再利用,能作为一个药效团作用于非传统的核糖体靶标,这极大拓展了经典抗生素再应用的新思路。
上述研究工作得到了国家自然科学基金项目、国家研发重点计划-合成生物学专项的支持。
论文信息:https://www.nature.com/articles/s41589-024-01685-3
Elena V. Aleksandrova#, Cong-Xuan Ma#, Dorota Klepacki#, Faezeh Alizadeh, Nora Vázquez-Laslop, Jian-Hua Liang*, Yury S. Polikanov*, Alexander S. Mankin*. Macrolones target bacterial ribosomes and DNA gyrase and can evade resistance mechanisms. Nature Chemical Biology, 2024, DOI: 10.1038/s41589-024-01685-3
附通讯作者简介:
梁建华,教授,博士生导师,北京市优秀人才,新药创制与绿色合成研究所所长,医药分子科学与制剂工程工信部重点实验室副主任。研究方向为药物化学,致力于治疗各种重大疾病的相关创新药物开发,研究兴趣包括抗耐药菌抗炎药物、抗神经退行性药物和抗糖尿病药物等领域。目前主持参与国家研发重点计划项目、科技创新2030重大项目、国家自然科学基金以及北京市自然科学基金等课题项目。在Cell Discovery、Eur. J. Med. Chem.、Bioorg. & Med. Chem.、Bioorg. & Med. Chem. Lett.、Curr. Med. Chem.、Curr. Top. Med. Chem.、J. Antibiotics等主流学术期刊上发表通讯作者论文30余篇,第一发明人授权中国专利11项、美国专利1项和PCT专利4项。
分享到:
